国内第Ⅲ相試験【STORK試験: 検証的試験】
社内資料:国内第Ⅲ相試験(STORK試験、CTD2.7.6.7)[承認時評価資料]
試験概要
- 目的
- :
- IVF/ICSIを受ける日本人患者を対象とする調節卵巣刺激において、採卵数に関してフォリトロピンベータ(遺伝子組換え(以下、フォリトロピンベータ))に対するレコベルの非劣性を検証する。
- 試験デザイン
- :
- 無作為化、実薬対照、評価者盲検、並行群間比較、多施設共同試験
- 対象
- :
- IVF/ICSIのための調節卵巣刺激を受ける日本人女性347例
- 試験方法
- :
- 実施医療機関及び刺激開始前60日以内に実施したスクリーニング時の血清AMH値(15pmol/L未満及び15pmol/L以上※1)を層別因子として、月経周期の2~3日目に、レコベル群又はフォリトロピンベータ群のいずれかに1:1で均等に無作為割付し、卵巣刺激を開始した。
血清AMH値が15pmol/L未満の被験者はレコベルの1日用量を12μg/日とし、15pmol/L以上の被験者は0.19~0.10μg/kgの範囲の連続変数に基づき、血清AMH値及び体重によりレコベルの1日用量を決定した。1日用量は刺激期間を通じて固定し、最高用量は12μg/日、最低用量は6μg/日とした。フォリトロピンベータの1日用量は投与開始から刺激5日目まで150IUで固定し、以降は卵巣反応に応じて75IU単位で調節可能としたうえで最高1日用量を375IUとした(フォリトロピンベータ150IUは15μgに相当する1))。レコベル及びフォリトロピンベータの投与期間は最長20日間とした。
併用薬の投与を含めた試験デザインを以下に示す。
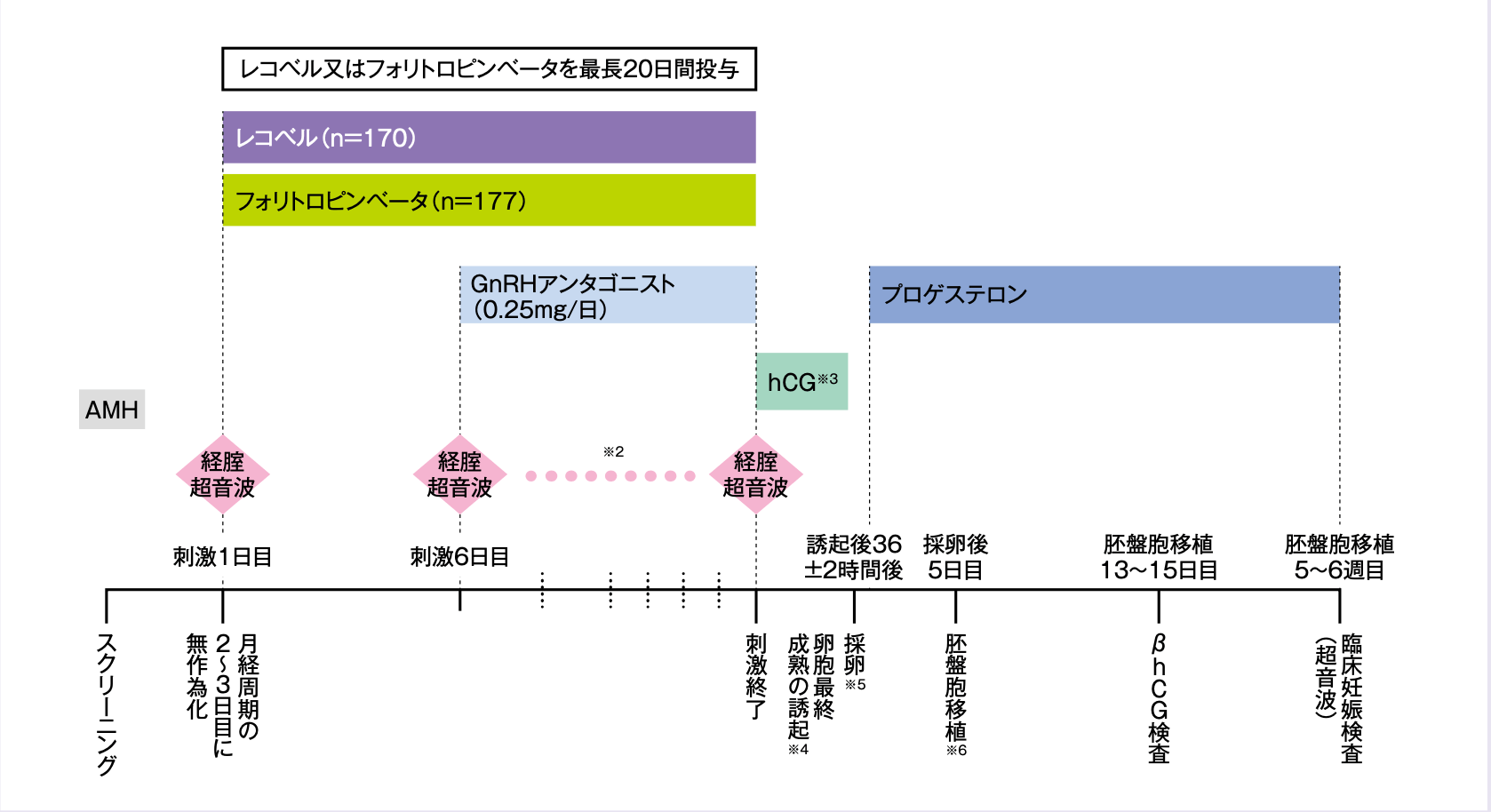
- 評価項目
- :
- (1)有効性
- <主要評価項目>
- 採卵数
- <重要な副次評価項目>
- 臨床妊娠率※7
- (2)安全性
- <副次評価項目>
-
- ・副作用の発現割合
- ・全卵巣過剰刺激症候群※8及び/又は早期発症型卵巣過剰刺激症候群に対する予防的介入の発現割合※9 等
- 解析計画
- :
- FASを主な解析対象集団として解析し、PP解析対象集団については補助的に解析した。主要評価項目である採卵数は、投与群及びAMH層を固定因子とする分散分析(ANOVA)を用いて解析した。平均値の投与群間差(レコベル-フォリトロピンベータ)とその両側95%信頼区間(CI)をモデルに基づき算出し、対立仮説(H1)に対する帰無仮説(H0)を検定した。FASにおいて両側95%CIの下限が非劣性マージンの-3.0個を上回った場合、帰無仮説は棄却され、レコベルのフォリトロピンベータに対する非劣性が検証されたと判断した。
なお、採卵数におけるCOS周期の中止、卵胞最終成熟の誘起の未実施及び採卵手技の未実施による欠測値については、0で補完した。
また、各投与群の各AMH層(高AMH層及び低AMH層)に対する治療効果の差について、投与群及びAMH層の交互作用を含めたANOVAを用いて解析した。さらに、AMH層別による部分集団解析を実施した(投与群のみを因子とした単純なモデル)が、各AMH層において非劣性を個別に検証する検出力はないため解析は補助的に行った。
重要な副次有効性評価項目及び他の副次有効性評価項目については、FAS及びPP解析対象集団を用いて、投与群間の比較を全被験者及び各AMH層で行った。特に重要な副次評価項目である臨床妊娠率については、Mantel-Haenszel法を用いて、各AMH層により調整した投与群間の差とその両側95%CIを求め推定した。なお、臨床妊娠率については、陽性と記録されていない場合、欠測値を陰性として補完した。
また、主要評価項目及び副次評価項目のAMH層因子別のサブグループ解析は事前に規定されていた。 -
※1 血清AMH値のng/mLからpmol/Lへの換算式:ng/mL×7.14=pmol/L
※2:刺激1及び6日目、その後は少なくとも隔日に実施し、15mm以上の大きさの卵胞が3個が確認された時点で、毎日来院することとした。
※3:直径が17mm以上の卵胞が3個以上みられた時点で尿由来ヒト絨毛性性腺刺激ホルモン(hCG)5000IUを投与し、卵胞最終成熟の誘起を行った。
※4:卵巣反応不良(刺激20日目までに直径17mm以上の卵胞が3個以上見られない)又は卵巣反応過剰(直径12mm以上の卵胞が25個以上)が認められた場合、周期を中止した。なお、直径12mm以上の卵胞が25~35個の範囲内である場合は、GnRHアゴニストを投与して、卵胞最終成熟の誘起を行うことができることとした。
※5:胚移植が予定されている被験者を対象に、黄体期管理のため採卵翌日から臨床妊娠の検査来院日までプロゲステロン腟錠100mgを1日3回投与した(プロゲステロン腟錠の用法及び用量:プロゲステロンとして1回100mgを1日2回又は3回、採卵日(又はホルモン補充周期下での凍結胚移植ではエストロゲン投与により子宮内膜が十分な厚さになった時点)から最長10週間(又は妊娠12週まで)腟内に投与する)。
※6:IVF/ICSIにより受精させた最も良好な胚盤胞1個を移植し、残りの胚盤胞は凍結した。
※7:胚移植後5~6週に子宮内又は子宮外を問わず少なくとも一つの胎嚢が認められるもの
※8:早期(誘起後9日以内)及び晩期(誘起後9日を超える)発症型の卵巣過剰刺激症候群
※9:早期発症型卵巣過剰刺激症候群に対する予防的介入を以下の通り定義した。
- ・卵巣反応過剰(直径12mm以上の卵胞が25個以上認められた場合)による周期の中止
- ・GnRHアゴニストによる卵胞最終成熟の誘起(直径12mm以上の卵胞が25~35個認められた場合)
- ・ドパミンアゴニストの投与(12mm以上の卵胞が20個以上ある被験者への予防的介入としてのみ検討する)
有効性
1)採卵数(主要評価項目)
採卵数(主解析、FAS)
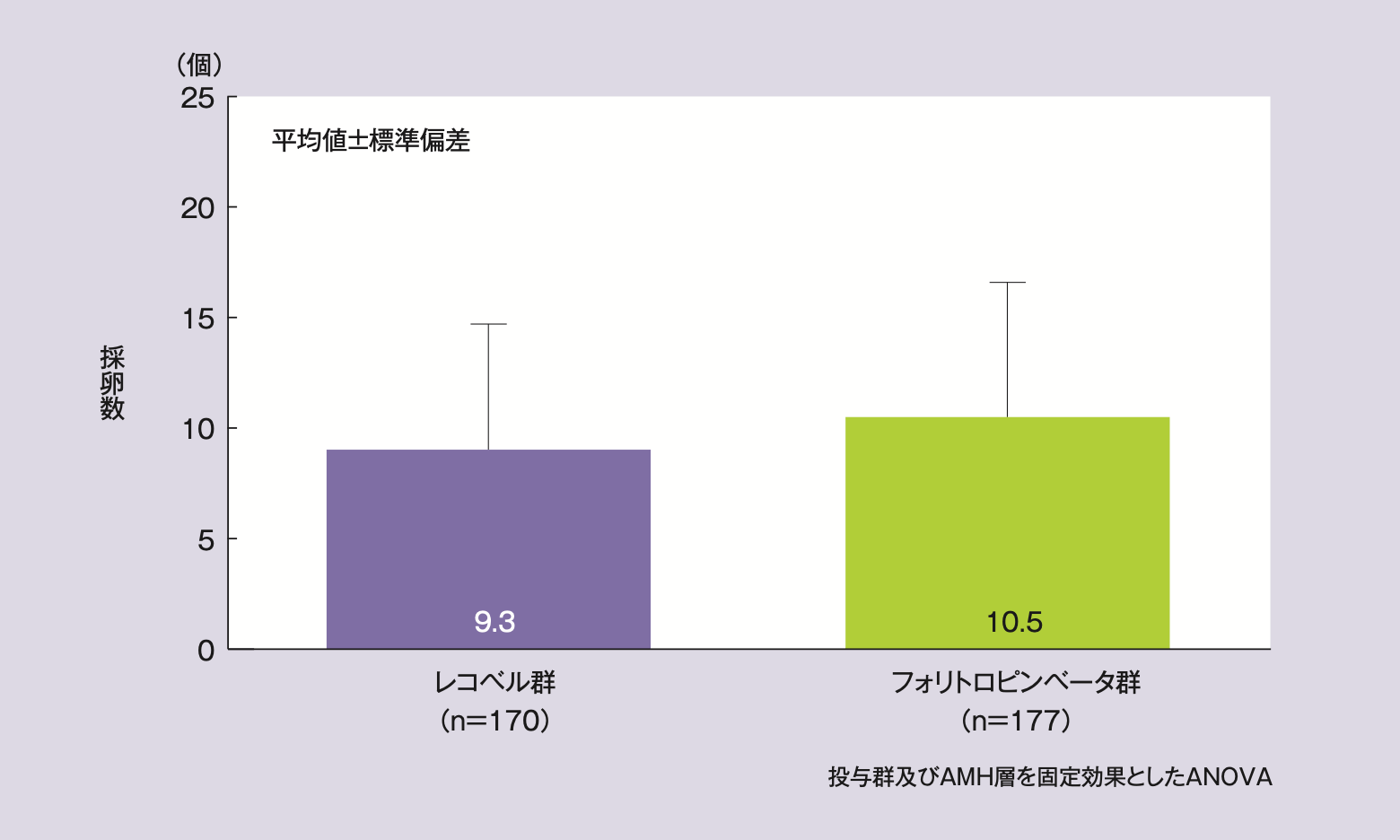
FASにおける採卵数(平均値±標準偏差)は、レコベル群9.3±5.4個、フォリトロピンベータ群10.5±6.1個であり、群間差及びその95%CIは-1.2個〔95%CI(-2.3,-0.1)、投与群及びAMH層を固定効果としたANOVA〕であった。95%CIの下限値は、事前に規定した非劣性マージンの-3.0個を上回り、採卵数についてレコベルのフォリトロピンベータに対する非劣性が検証された。
全被験者の採卵数
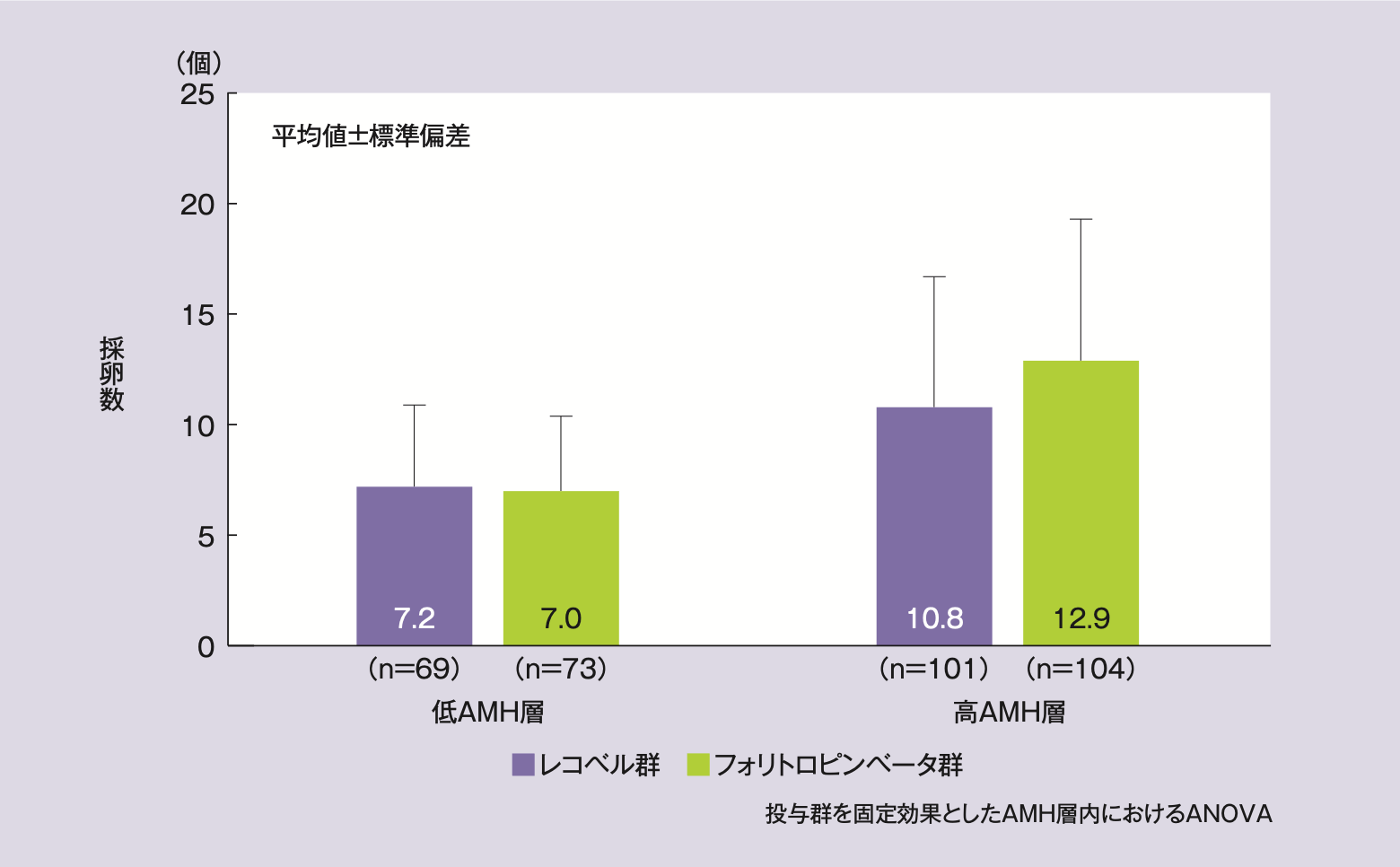
AMH層別採卵数(追加解析、FAS:サブグループ解析)
低AMH層の採卵数(平均値±標準偏差)は、レコベル群7.2±3.7個、フォリトロピンベータ群7.0±3.4個であり、群間差及びその95%CIは0.1個〔95%CI(-1.0,1.3)〕※1:投与群及びAMH層を固定効果としたANOVAであった。高AMH層の採卵数(平均値±標準偏差)は、レコベル群10.8±5.9個、フォリトロピンベータ群12.9±6.4個であり、群間差及びその95%CIは-2.2個〔95%CI(-3.9,-0.5)〕※1であった。
※1:投与群を固定効果としたAMH層内におけるANOVA
AMH層別の採卵数
レコベル群及びフォリトロピンベータ群の採卵数における血清AMH値依存性の差を、投与群-AMH層を交互作用項として含めたANOVAモデルで検証した。
採卵数に対し、投与群及びAMH層に統計学的に有意な交互作用が認められ(p=0.046)、血清AMH値に基づくレコベルの個別化用量は、対照であるフォリトロピンベータと異なる方法により卵巣反応を調節することが示された。
採卵数に対するAMH層で調整した群間比較及び投与群-AMH層の交互作用(FAS)

※2:投与群、AMH層及び投与群-AMH層の交互作用項を固定効果として含めたANOVAによる比較
※3:ANOVAモデルにおける投与群-AMH層の交互作用に対するp値
2)臨床妊娠率(重要な副次評価項目、FAS:サブグループ解析を含む)
臨床妊娠率はレコベル群25.3%(43/170例)、フォリトロピンベータ群23.7%(42/177例)であり、群間差及びその95%CIは1.6%〔95%CI(-7.5%,10.6%)、AMH層で調整されており、各AMH層内で得られたリスク差を関連付けるMantel-Haenszel法及び各AMH層の正規近似〕であった。AMH層別のサブグループ解析ではレコベル群の低AMH層21.7%(15/69例)、高AMH層27.7%(28/101例)、フォリトロピンベータ群の低AMH層24.7%(18/73例)、高AMH層23.1%(24/104例)であった。
安全性
1)副作用の発現割合(副次評価項目、安全性解析対象集団)
副作用の発現割合は、レコベル群18.8%(32/170例)、フォリトロピンベータ群25.4%(45/177例)であった。
主な副作用(いずれかの群で2%以上)は、卵巣過剰刺激症候群がレコベル群10.6%(18/170例)、フォリトロピンベータ群19.2%(34/177例)、卵巣腫大がそれぞれ2.9%(5/170例)及び2.3%(4/177例)、骨盤液貯留がそれぞれ2.4%(4/170例)及び1.7%(3/177例)であった。
本試験で死亡例は認められず、重篤な副作用はフォリトロピンベータ群2例(いずれも卵巣過剰刺激症候群)に認められた。
中止に至った有害事象は、レコベル群13例(卵巣過剰刺激症候群8例、プロゲステロン増加3例、インフルエンザ、ウイルス性上気道感染各1例)に、フォリトロピンベータ群18例(卵巣過剰刺激症候群14例、卵巣腫大2例、プロゲステロン増加、卵管水腫各1例)に認められた。
2)全卵巣過剰刺激症候群及び/又は早期発症型卵巣過剰刺激症候群に対する予防的介入の発現割合(副次評価項目、安全性解析対象集団)
発現した卵巣過剰刺激症候群を系統的に分類するためGolan分類を適用した(Golan分類についてはこちらを参照)。
全卵巣過剰刺激症候群(全グレード)はレコベル群11.2%(19/170例)、フォリトロピンベータ群19.8%(35/177例)に認められた。
全卵巣過剰刺激症候群(全グレード)及び/又は予防的介入が認められた被験者の割合はレコベル群11.8%(20/170例)、フォリトロピンベータ群22.0%(39/177例)であった。
8. 重要な基本的注意(一部抜粋)
8.2 調節卵巣刺激をする際に卵巣への刺激が過剰になることがある。
以下の点に留意し、卵巣過剰刺激症候群の発現が予想された場合は、本剤の投与を中断し、少なくとも4日間は性交を控え、避妊するように指導すること。
- ・患者の自覚症状の有無(初期の警告的な徴候として、重度の骨盤痛、悪心及び嘔吐)
- ・急激な体重増加の有無(初期の警告的な徴候)
- ・卵巣腫大の有無(内診の他、超音波検査、血清エストラジオール値検査等)
卵巣過剰刺激症候群は本剤投与終了後に発現し、急速に(24時間から数日以内)進行して重篤化することがあるため、投与後少なくとも2週間の経過観察が必要である。多くの場合、投与後7日から10日経過した時期に最も症状が重くなる。通常、月経開始とともに自然に解消するが、妊娠した場合は、より重度になる。[1.、11.1.1参照]
11.1 重大な副作用
11.1.1 卵巣過剰刺激症候群(10.6%)
軽度又は中等度の卵巣過剰刺激症候群(10.6%)では一過性下腹部不快感、軽度悪心、嘔吐、下痢及び腹部膨満等がみられ、卵巣過剰刺激症候群の進行によって症状の持続や悪化が認められる。重度の卵巣過剰刺激症候群では、腹痛、腹部膨満、重度の卵巣腫大、体重増加、呼吸困難、乏尿、及び持続する悪心・嘔吐・下痢などの消化管症状等の症状がみられ、臨床的評価では血液量減少症、血液濃縮、電解質失調、腹水、腹膜腔出血、胸水、胸水症、呼吸困難、心囊液貯留、血栓塞栓症が認められる場合がある。重度の卵巣過剰刺激症候群(0%)では、卵巣茎捻転、卵巣破裂による卵巣出血、肺塞栓症、虚血性脳卒中、心筋梗塞、成人呼吸窮迫症候群等の合併症により重篤化することがある。重度の卵巣過剰刺激症候群が認められた場合には直ちに投与を中止し、入院させて適切な処置を行うこと。[1.、8.2参照]
1)PUREGON. Summary of Product Characteristics.
https://www.ema.europa.eu/en/documents/product-information/puregon-epar-product-information_en.pdf(2021年9月時点)
 は、フェリング・ファーマ株式会社が提供する、医療関係者向け 領域専用サイトの総称です。
は、フェリング・ファーマ株式会社が提供する、医療関係者向け 領域専用サイトの総称です。 は、
は、 会員登録がお済みでない方
会員登録がお済みでない方


