国内第III相試験では、新鮮胚移植の患者108例に対し、ルティナス1回1錠(100mg錠)1日2回投与(BID)群又は1日3回投与(TID)群に無作為に分け、プロゲステロン血中濃度、妊娠率等の有効性と安全性について検討しました。胚移植症例90例において、投与5週目で胎児及び胎児心拍の確認ができた症例の割合「継続妊娠率」は22.2%でした。統計学的検討(有意差検定)は行っていないものの、1日3回投与群にて妊娠率が高い傾向が示されました。
【試験デザイン】
多施設共同、無作為化、非盲検、並行群間試験
【 対 象 】
20~42歳のIVF-ET又はICSIを受ける閉経前の女性
・Intention-to-treat(包括解析:ITT)解析対象集団*:108例
ルティナス100mg1日2回投与群( BID群):54例
ルティナス100mg1日3回投与群( TID群):54例
・Full Analysis Set(最大解析対象集団:FAS)**:94例( BID群 46例、TID群 48例)
・胚移植例:90例(BID群 43例、TID群 47例)
・安全性解析対象集団:108例( BID群 54例、TID群 54例)
* 無作為に割付けされ治験薬を投与された患者をITT解析対象集団に含めた。
**主要な有効性解析対象集団。試験を終了した被験者をFASに含めた。
【 方 法 】
投与前期:
スクリーニング後、GnRHアゴニストによる下垂体ダウンレギュレーション、又はGnRHアンタゴニストによる早発黄体形成ホルモンサージの防止により、調節卵巣刺激、排卵誘発を行った。
投与期
:
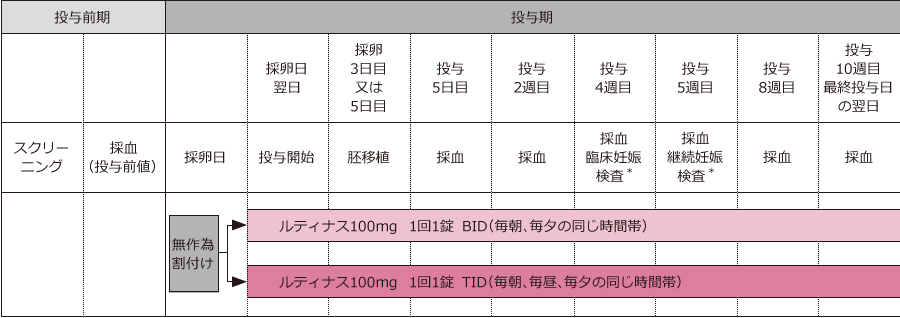
ルティナスの投与は、採卵日の翌日から開始した。対象患者をルティナス100mgの1日2回投与(BID群)及び1日3回投与(TID群)に無作為に割付け、最長10週間連日投与した。採卵3日目又は5日目に治験実施医療機関の基準に従い胚移植を実施した。投与4及び5週目に妊娠検査を実施し、妊娠が確認できた場合は投与を継続し、妊娠が確認できない場合はその時点で安全性の評価を含むフォローアップを実施し、当該患者の試験を終了した。
【評価項目】
主要評価項目
:
投与5日目の血清中プロゲステロン濃度が10ng/mL*以上である患者の割合
:
継続妊娠率[投与5週目の経腟超音波検査(TVU)による胎児及び胎児心拍の確認]
副次評価項目
:
臨床妊娠率(投与4週目のTVUによる胎嚢確認)
:
β-hCG検査による陽性率
:
血清中プロゲステロン濃度(投与2、4、5、8週目、試験終了時の血清中プロゲステロン濃度)が10ng/mL*以上である患者の割合
【解析計画】
有 効 性
:
FAS及びPP解析対象集団を用いて解析した。
プロゲステロン濃度(5日目)が10ng/mL以上の患者割合:
MEGASET試験2)での患者割合(99.84%)との差の両側95%CIが-10%を下回らないことを確認した。
継続妊娠率
:
両側95%CIを算出した。
安 全 性
:
安全性解析対象集団を用いて記述統計量にて要約した。
【安 全 性】
副作用発現率は8.3%(9/108例)であり、投与群別にみるとルティナスBID群で3.7%(2/54例)、ルティナスTID群で13.0%(7/54例)であった。
100mg BID群でみられた副作用は、傾眠及び肝機能検査異常で各1.9%(各1/54例)に認められた。100mgTID群では、頭痛及び性器出血が各3.7%(各2/54例)で、次いで傾眠、下痢、腹部膨満及び便秘が各1.9%(各1/54例)に認められた。
10ng/mLは黄体機能不全の診断における血清中プロゲステロン濃度の基準値として良く知られている。生殖補助医療における黄体期血清中プロゲステロン濃度の基準値については、黄体機能不全の基準値のように明確に定められたものはない。一方、MEGASET試験2)(欧州におけるゴナドトロピン製剤の大規模比較試験)において黄体補充を行った際の黄体期(採卵5日目)の血中プロゲステロン濃度が、ほぼ全例において10ng/mL以上であることが確認されている。そこで、これを既存対照(ヒストリカルコントロール)とみなし、本試験においてもこれに倣って黄体期の血中プロゲステロン濃度が10ng/mL以上である患者の割合を主要評価項目とした。
 は、フェリング・ファーマ株式会社が提供する、医療関係者向け 領域専用サイトの総称です。
は、フェリング・ファーマ株式会社が提供する、医療関係者向け 領域専用サイトの総称です。 は、
は、 に会員登録することでご利用いただけます。
に会員登録することでご利用いただけます。 会員登録がお済みでない方
会員登録がお済みでない方



![継続妊娠率[主要評価項目]](/res/front/assets/img/photo_medicine_lutinus08.png)
